Denna publikation publicerades för mer än 5 år sedan. Kunskapen kan ha förändrats genom att ny forskning tillkommit och att den visar på andra resultat. Det är dock mindre troligt att resultat med starkt vetenskapligt stöd förändras, även om nya studier tillkommer.
Humant papillomvirus-test eller upprepad cellprovtagning vid låggradiga cellförändringar på livmoderhalsen
Är du patient/anhörig? Har du frågor om egna eller anhörigas sjukdomar – kontakta din vårdgivare eller handläggare.
Inledning
Humant papillomvirus (HPV)-infektioner kan läka ut spontant men kroniska infektioner med vissa HPV-typer kan ge upphov till cellförändringar i livmoderhalsen, som obehandlade kan utvecklas till cancer.
För kvinnor som redan är diagnostiserade med låggradiga cellförändringar kan ett positivt HPV-test tyda på att de löper en högre risk att ha eller utveckla höggradiga cellförändringar. Ett negativt resultat skulle däremot betyda att kvinnan har en lägre risk att ha eller utveckla höggradiga cellförändringar.
Här sammanfattar och kommenterar SBU en systematisk kunskapsöversikt från Cochrane Collaboration om betydelsen av HPV-test i triage av patienter med låggradiga cellförändringar på livmoderhalsen.
Originalrapport
SBU:s sammanfattning
Cochrane-översikten visar att HPV-test (HC2) är mer känsligt och lika träffsäkert som upprepat cellprov vid utredning av kvinnor med den lägsta graden av cellförändringar (ASCUS). För kvinnor med näst lägsta graden (LSIL) är HPV-testet känsligare än upprepat cellprov men förmågan att utesluta kvinnor utan höggradiga cellförändringar är påtagligt lägre. Cochrane-översikten stärker de tidigare svenska ställningstagandena att triage med HPV test är en möjlig handläggning av kvinnor med ASCUS och LSIL.
SBU:s kommentarer
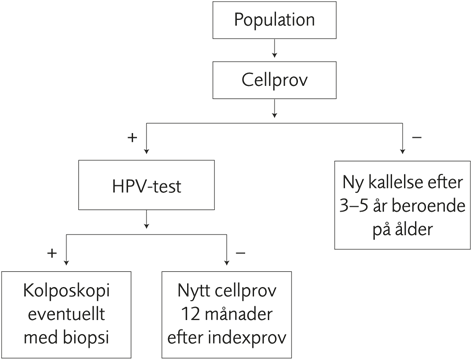
- Uppföljning av låggradiga cellförändringar som påvisas vid gynekologisk cellprovtagning är ett stort kliniskt problem. I Sverige ställs årligen mer än 30 000 diagnoser med låggradig cellförändring på gynekologiska cellprov. I Sverige finns idag två handläggningsmöjligheter: att utreda alla dessa kvinnor med gynekologisk undersökning (kolposkopi) eller att endast utreda dem som är positiva för HPV. I en del landsting utreds alla, i andra landsting görs ”triagning” med HPV-test av alla och på de flesta håll används HPV-test för triagning i åldersgruppen 35 år och äldre.
- Rapporten har begränsats till ett äldre HPV-test (HC2), men flertalet HPV-test som används i Sverige har jämförbar prestanda. Flertalet HPV-tester är idag baserade på PCR, men hybridiseringsmetoder som HC2 är fortfarande brett använda. Vanligen används samma cellprov som används till den cytologiska undersökningen.
- Handläggning med triage med upprepat cellprov är inte god vård i Sverige för kvinnor över 27 års ålder på grund av låg sensitivitet (risk att missa patienter med hög cancerrisk). Rapporten styrker dock de tidigare svenska ställningstagandena att triage med HPV-test, men inte med cytologi, är en möjlig handläggning för dessa patienter.
- I samverkan med Socialstyrelsen håller SBU för närvarande på med att ta fram ett kunskapsunderlag om primär screening för livmoderhalscancer och cellprov med analys för HPV och cytologi. Socialstyrelsen kommer att använda kunskapsunderlaget vid bedömning av screeningprogram för livmoderhalscancer.
- Rapporten saknar hälsoekonomisk utvärdering.
Sammanfattning av originalrapporten
Om studierna i originalrapporten
I Cochrane-rapporten inkluderades 42 studier, varav tre var randomiserade kontrollerade och i de övriga studierna tillämpades en ”split-sample”-strategi där varje kvinna undersöktes med både HPV-testet och en referensmetod (dvs varje kvinna utgjorde sin egen kontroll). Hälften av studierna är utförda i Europa och övriga studier är utförda i Kanada, USA, Kina, Sydkorea, Taiwan och Thailand. I studierna ingick 23 179 kvinnor med låggradiga cellförändringar, av vilka 13 196 hade lätt skivepitelatypi (ASCUS = atypical cells of undetermined significance) och övriga 9 983 hade lätt dysplasi (LSIL = low grade squamous intraepithelial lesion).
I samtliga studier jämfördes indextestet (HPV-testet) med en referensmetod (kolposkopi eventuellt med biopsi). I rapporten inkluderades endast studier som använde HPV-testet ”hybrid Capture 2” (HC2 HPV DNA). I en del studier jämfördes dessutom indextestet med ett jämförande indextest (ett upprepat cytologprov). Genom att jämföra HPV-testet med en etablerad metod kan man utvärdera HPV-testets relativa diagnostiska tillförlitlighet.
De kvinnor som ingick i studierna hade alla diagnostiserats med låggradiga cellförändringar med hjälp av ett initialt cytologprov. I 39 studier utreddes patienterna vidare med ett HPV-test och en referensmetod (kolposkopi eventuellt med biopsi). I 10 studier togs även ett upprepat cytologprov, vanligen mellan 3 och 12 månader efter det initiala cytologprovet.
Rapportens primära utfallsmått var relativ sensitivitet och specificitet av HPV-testet jämfört med ett upprepat cytologprov för att påvisa närvaron av underliggande höggradiga cellförändringar (CIN 2+ eller CIN 3+). Endast studier som utvärderade både indextestet och det jämförande indextestet ingick i beräkningen av dessa mått.
De sekundära utfallsmåtten var absolut sensitivitet och specificitet av HPV-testet oavsett om ett upprepat cytologprov togs. Samtliga studier ingick i beräkningen av dessa mått.
Resultat
HPV-testets relativa sensitivitet och specificitet
HPV-test och upprepat cytologprov jämfördes med avseende på deras sensitivitet och specificitet. Den absoluta sensitiviteten och specificiteten beräknades separat för varje metod och därefter utvärderades den relativa sensitiviteten och specificiteten av HPV-testet.
För kvinnor med ASCUS-diagnos
HPV-test har 27 procent högre sensitivitet för upptäckt av CIN 2+ (relativ sensitivitet 1,27; 95 % konfidensintervall (KI) 1,16 till 1,39). Metodernas specificitet var likvärdiga vid det lägsta cut off-värdet (ASCUS+) (relativ specificitet 0,99; 95 % KI 0,97 till 1,03). HPV-testets relativa specificitet minskar med ökat cytologiskt cut off-värde.
Tabell 1 HPV-test.
| Utfall | Antal studier | Sensitivitet (95% KI) | Specificitet (95% KI) |
| CIN 2+ | 10 | 90,9% (85,7 till 94,4%) | 60,7% (52,9 till 68,0%) |
| CIN 3+ | 4 | 94,8% (89,3 till 97,5%) | 56,6% (39,4 till 72,3%) |
Tabell 2 Upprepat cytologprov.
| Utfall | Cut off | Antal studier | Sensitivitet (95% KI) | Specificitet (95% KI) |
| CIN 2+ | ASCUS+ | 10 | 71,5% (62,9 till 78,8%) | 68,4% (59,9 till 75,8%) |
| LSIL+ | 6 | 44,1% (33,3 till 55,5%) | 90,1% (83,3 till 94,4%) | |
| HSIL+ | 5 | 15,8% (6,5 till 33,6%) | 98,3% (96,7 till 99,1%) | |
| CIN 3+ | ASCUS+ | 4 | 77,9% (64,0 till 87,6%) | 57,4% (40,4 till 73,0%) |
| LSIL+ | 4 | 53,5% (17,8 till 85,9%) | 79,9% (73,4 till 85,2%) | |
| HSIL+ | 4 | 33,2% (6,1 till 79,2%) | 95,6% (93,6 till 97,1%) |
För kvinnor med LSIL(CIN 1)-diagnos
HPV-test har 23 procent högre sensitivitet för detektion av CIN 2+ (relativ sensitivitet 1,23; 95 % KI 1,06 till 1,43). Specificiteten av HPV-test var 34 procent lägre jämfört med upprepat cytologi vid den lägsta cytologisk cut off-nivån (ASCUS+) (relativ specificitet 0,66; 95 % KI 0,58 till 0,75). Vid högre cytologiska cut off-nivåer har HPV-test ännu lägre relativ specificitet jämfört med upprepat cytologprov.
Tabell 3 HPV-test.
| Utfall | Antal studier | Sensitivitet (95% KI) | Specificitet (95% KI) |
| CIN 2+ | 6 | 96,2% (91,4 till 98,3%) | 27,7% (20,9 till 35,7%) |
| CIN 3+ | 4 | 97,5% (69,6 till 99,8%) | 24,8% (7,3 till 58,1%) |
Tabell 4 Upprepat cytologprov.
| Utfall | Cut-off | Antal studier | Sensitivitet (95% KI) | Specificitet (95% KI) |
| CIN 2+ | ASCUS+ | 6 | 77,1% (59,5 till 88,5%) | 51,2% (34,5 till 67,6%) |
| LSIL+ | 4 | 62,1% (33,4 till 84,3%) | 66,9% (51,5 till 79,4%) | |
| HSIL+ | 4 | 31,6% (18,2 till 49,0%) | 96,6% (93,6 till 98,3%) | |
| CIN 3+ | ASCUS+ | 4 | 84,6% (48,6 till 97,0%) | 44,4% (16,0 till 76,9%) |
| LSIL+ | 4 | 71,6% (33,4 till 92,7%) | 61,8% (33,1 till 84,1%) | |
| HSIL+ | 4 | 41,9% (24,8 till 61,2%) | 93,8% (86,1 till 97,4%) |
Slutsatser enligt originalrapporten
HPV-test (HC2) har högre sensitivitet och specificitet än upprepat cellprov i triagen av kvinnor med ASCUS. För kvinnor med LSIL (CIN 1) har HPV-testet bättre sensitivitet än upprepat cellprov men specificiteten, det vill säga förmågan att utesluta kvinnor utan höggradiga cellförändringar är påtagligt lägre.
SBU:s granskning av originalrapporten
Vid SBU:s kvalitetsbedömning av originalrapporten användes en granskningsmall för systematiska översikter (AMSTAR) [1]. Granskningen visade att litteratursökning, studieurval och dataextraktion uppfyllde definierade kvalitetskrav för en systematisk översikt.
Bindningar och jäv
Sakkunniga och granskare har i enlighet med SBU:s krav inlämnat deklaration rörande bindningar och jäv. Dessa dokument finns tillgängliga på SBU:s kansli. SBU har bedömt att de förhållanden som redovisas där är förenliga med kraven på saklighet och opartiskhet.
Faktarutor
| Faktaruta 4 Diagnostiska studier |
| I dessa studier utvärderas det diagnostiska tillförlitligheten av ett test, det vill säga dess förmåga att skilja på individer med sjukdom och dem utan sjukdom. Testet som ska utvärderas kallas för indextest. Ibland jämförs ett nytt test med ett test som utgör standard i klinisk praxis (jämförande indextest). Tillförlitligheten hos indextestet bedöms i jämförelse med en referensmetod som representerar det bästa tillgängliga sättet för att påvisa sjukdomen eller tillståndet ifråga. Förutom information om var i den diagnostiska kedjan det nya testet ska ingå, är det viktigt att veta vilka tester eller annan information som finns tillgängliga i den undersökta populationen, innan tillförlitligheten hos ett nytt test ska undersökas. Om till exempel endast patienter med ett visst positivt testresultat ingår då det nya testet ska göras, har sammansättningen i populationen förändrats. Sannolikheten för sjukdom efter ett positivt testutfall ökar, vilket påverkar det nya testets sensitivitet och specificitet. Sensitivitet och specificitet är två grundläggande mått som används för att beskriva indextestets tillförlitlighet: Sensitivitet = Sannolikheten för positivt testresultat när man har sjukdomen. Specificitet = Sannolikheten för negativt testresultat när man är frisk. Cut off-värde, eller tröskelvärde, är en gräns som väljs för att skilja mellan ”sjukdom” och ”ej sjukdom”. Hur man väljer denna gräns påverkar antalet falska positiva/negativa och därmed påverkar sensitiviteten och specificiteten. I den aktuella studien har CIN 2+ = CIN 2 eller högre grad av dysplasi eller cancer, respektive CIN 3+ använts som gräns för sjukdom. Läs mer om diagnostiska studier i SBU:s metodbok, Utvärdering av metoder i hälso- och sjukvården. |
Lästips
- Svensk förening för obstetrik och gynekologi. Cervixcancerprevention: riktlinjer för utredning, behandling och uppföljning av cervikal intraepitelial neoplasi (CIN). Stockholm: Svensk förening för obstetrik och gynekologi; 2010.
Referenser
- Shea BJ, Grimshaw JM, Wells GA, Boers M, Andersson N, Hamel C, et al. Development of AMSTAR: a measurement tool to assess the methodological quality of systematic reviews. BMC Med Res Methodol 2007;7:10.
- Poljak M, Cuzick J, Kocjan BJ, Iftner T, Dillner J, Arbyn M.Nucleic acid tests for the detection of alpha human papillomaviruses. Vaccine 2012 Nov 20;30 Suppl 5:F100-6. doi: 10.1016/j.vaccine.2012.04.105.
- Woodman CB, Collins SI, Young LS. The natural history of cervical HPV infection: unresolved issues. Nat Rev Cancer 2007;7:1111-22.
Projektgrupp och granskare
Projektgrupp
Sakkunnig
Joakim Dillner, professor i Infektionsepidemiologi, Karolinska Institutet
SBU
Naama Kenan Modén, projektledare
Mikael Nilsson, projektledare
Sara Fundell, projektadministratör
Madelene Lusth Sjöberg, projektadministratör
Granskare
Björn Strander, överläkare vid Regionalt cancercentrum Väst. Ordförande Nationella expertgruppen för cervixcancerprevention
Projektsamordnare
Mikael Nilsson, SBU
 Statens beredning för medicinsk och social utvärdering
Statens beredning för medicinsk och social utvärdering